表1. 所有患者的临床特征
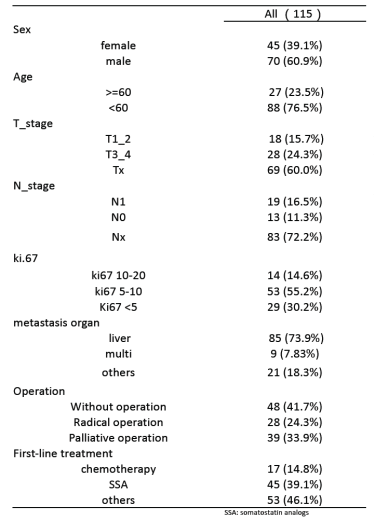
表2. 单因素和多因素COX回归分析
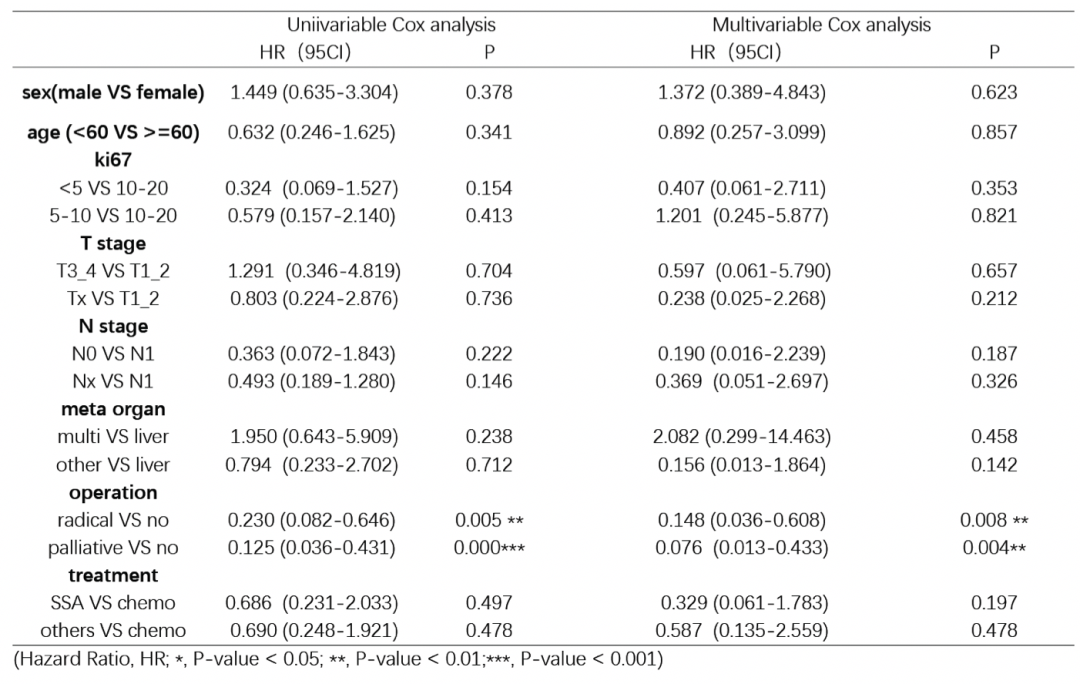
图1. OS的Kaplan-Meier曲线:(A) 转移性非功能性G2 pNET;
(B) 一线治疗亚组;(C) 手术类型亚组
白春梅教授:这篇来自北京协和医院的单中心真实世界研究报道,对中国人群神经内分泌肿瘤的治疗干预经验进行了分享。研究者选择了中国人群诊出率最高的pNET亚组进行分析,共纳入了2001年至2019年在北京协和医院肿瘤内科进行诊疗的115例伴有远处转移的非功能性pNET 患者。研究结果显示,经过内科、外科等多学科治疗的非功能型转移性pNET患者5年生存率79.36%,10年生存率也到达70%。类比JAMES YAO教授发表于2008年基于美国SEER数据库流行病学研究结果[1]转移性pNET中位生存期27月,3年、5年、10年生存率仅有42%,27%,11%,生存率获得巨大提升。这提示我们,现阶段的多学科规范化系统性治疗带给患者的生存收益不可忽视。而治疗手段的进步存在于哪些方面呢?第一,适时的外科干预,手术几乎是既往可以治愈神经内分泌肿瘤的唯一手段,随着手术技术的提升根治性切除已经在部分伴肝脏寡转移的病例开展,而姑息性减瘤手术也成为了转移性pNET的一项重要治疗手段。在我们的真实世界研究结果中,相较于未接受手术治疗的患者,接受根治性切除或姑息减瘤手术的患者具有明确的生存获益。接受根治性切除和姑息性手术的患者死亡风险降低85.2%和92.4% 。第二,药物全身治疗的进展。2009年PROMID研究以及2014年CLARINET研究验证长效奥曲肽和兰瑞肽 Autogel在神经内分泌肿瘤治疗中的抗肿瘤作用;2010年,2011年mTOR抑制剂依维莫司和VEGFR抑制剂舒尼替尼也弥补了靶向治疗在神经内分泌肿瘤的空白,近两年索凡替尼等一些新型靶向药物陆续开展神经内分泌治疗研究,丰富了靶向治疗的选择;以CAPTEM为主的化疗方案也以不同的药物组合模式在全球范围内开展研究并相继应用于临床。丰富的内科全身治疗方案给pNET这种高度特异性肿瘤的整个诊疗过程提供了多种的选择,并直接给予患者更好的生存质量和更长的生存期。在我们的研究中,以化疗作为起始治疗方案的患者中位生存期为5627天,而以SSA作为起始治疗方案的中位生存期尚未达到,未得到明确的统计学差异,这可能与ki67指数或瘤负荷或进展速度以及后续治疗等因素影响有关。第三,TAE技术及核医学诊疗技术的应用。TAE可以阻断肝转移病灶的肿瘤动脉血供,核医学领域Ga68 及PRRT可以利用神经内分泌肿瘤表达生长抑素受体,特异性的对肿瘤细胞进行定位诊断,甚至进行同位素治疗。综上所述,与1973-2004年间美国SEER数据库的流行病学报告相比,手术、药物及核医学等综合治疗带给神经内分泌肿瘤患者的获益是巨大的,这直接导致转移性pNET生存率的提高。
这篇壁报交流的摘来自是一项来自北京协和医院的单中心回顾性真实世界研究,仅选取整项研究中的非功能性pNET亚组的分析结果进行报道。作为回顾性真实世界研究,虽然在手术与药物治疗亚组中存在选择偏倚,但在真实医疗环境下,真实世界研究的证据更进阶临床实际,能直接为真实世界的医疗决策提供全面可信的参考依据。
参考文献:1.Yao JC, Hassan M, Phan A, One hundred years after "carcinoid": epidemiology of and prognostic factors for neuroendocrine tumors in 35,825 cases in the United States. J Clin Oncol. 2008 Jun 20;26(18):3063-72. doi: 10.1200/JCO.2007.15.4377.
H19: pNET根治性切除术后,早期复发预测危险因素模型及SSA术后辅助治疗
pNET具有生长惰性、异质性高和恶性潜能多变等特点,而识别出影响pNET根治性切除术后早期复发和患者预后的独立预测因素非常重要。复旦大学肿瘤医院虞先濬教授团队开展的本研究,分析了接受胰腺切除术的分化良好的319例pNET患者(队列A,建模队列)和106例的患者(队列B,验证队列)的临床相关参数。
结果显示:G3 pNET、胰管扩张和胰周神经浸润,与根治性切除术后pNET早期复发(1.5年内)显著相关(分别为P= 0.019、P< 0.001和P< 0.001),是无复发生存的独立预测因素。基于这些高危因素,该研究建立了一个全新危险因素模型——R模型评分系统,它能够用于预测根治性切除术后的早期复发(P< 0.001,HR = 15.02,95% CI 5.76 - 39.19)。R模型评分系统具有良好的预测准确性,C-index 0.853,高于AJCC TNM分期(0.713)。同时, 建立了一套结合了R模型评分和TNM分期的综合分期系统,可提高预测的准确性。
该研究结果表明,SSA术后辅助治疗可显著减少具有G3 pNET、胰管扩张和胰周神经浸润这三种危险因素患者的复发(P< 0.001),并延长生存期(P= 0.021)。
白春梅教授:摘要H19来自复旦大学肿瘤医院虞先濬教授团队,探讨了 pNET根治性切除术后复发高危因素和术后辅助治疗,这一直是近年来的研究热点。该研究建立了一个全新的以G3 NET、胰管扩张、胰周神经侵犯这三个高危因素为基础的、有效预测早期复发的R模型评分系统,同时,验证了SSA术后辅助治疗可显著减少具有这三种高危因素患者的复发,并延长生存期。R模型评分系统的建立,对临床识别早期复发风险的患者具有重要价值,需要临床进一步验证,同时该研究也为SSA术后辅助治疗积累了更多的临床证据。
H15:SSA一线治疗晚期胰腺和肠道神经内分泌肿瘤, 中位PFS达31个月
该回顾性研究纳入了120例接受SSA一线治疗(长效奥曲肽和兰瑞肽)的晚期高/中分化的胰腺及肠道NET患者,主要终点为根据RECIST 1.1评价的无进展生存期(PFS),次要终点为临床因素与总生存期之间的相关性。结果显示,120例患者平均年龄56.59 ± 12.59岁,瘤体大小5.97 ± 3.82 cm,起源部位:胰腺35.83%,中肠36.67%,后肠20.83%,其他6.67%。79.50 %的患者使用长效奥曲肽作为一线治疗。所有患者的中位PFS为31.62 个月,其中pNET PFS为24.5 ± 19.5 (3.77 - 97) 个月。奥曲肽组中位OS 117.20个月,兰瑞肽组中位OS 94.60个月,未观察到不同SSA之间OS的差异(P=0.12)。单变量分析未显示不同性别、年龄、临床分期、ECOG体能状态的PFS差异。
图2 Kaplan-Meier PFS、OS曲线
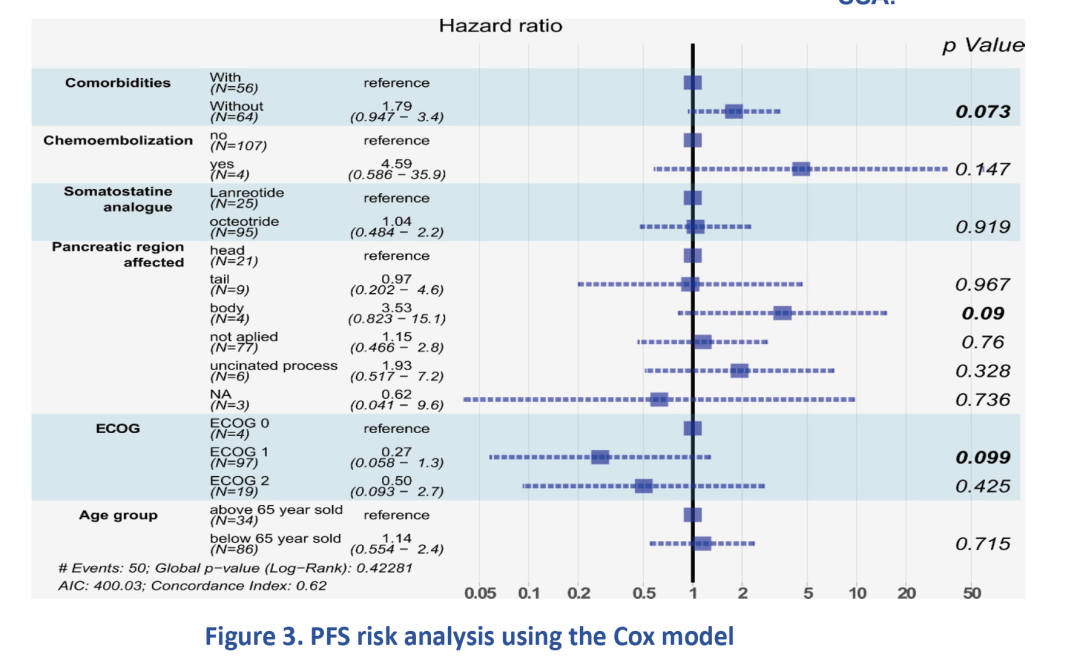
图3 应用Cox模型进行PFS风险分析
表3 PFS相关的临床因素分析
白春梅教授:摘要H15,回顾性探讨了SSA(长效奥曲肽和兰瑞肽)一线治疗晚期胰腺和肠道神经内分泌肿瘤疗效。我们知道,长效奥曲肽Promid研究纳入的是12月内进展的中肠来源的NET患者,对于胰腺和后肠NET,长效奥曲肽作为晚期一线治疗的证据相对有限。而该研究纳入的120例患者中,发病部位胰腺占35.83%,后肠20.83%。约95名使用长效奥曲肽作为一线治疗。所有患者mPFS为31.62 个月,其中pNET mPFS为24.5个月,奥曲肽组中位OS 117.20个月。该研究入组时患者是进展还是稳定未描述,ki67中位数2%,结果再次表明SSA一线治疗高分化神经内分泌瘤患者具有良好疗效。
H14: SSA加量治疗进展性胰腺或中肠NET的疗效、安全性和生活质量(QoL): CLARINET FORTE研究结果
这项前瞻性、单臂、非盲、在欧洲进行的2期临床研究,对过去2年接受标准兰瑞肽autogel(LAN)治疗超过24周,并出现进展的转移性或局部晚期不可切除的G1/2 pNET(n=48)或中肠NET患者(n=51),给与LAN120mg/14天,持续48周(pNET)或96周(中肠NET) (或直到疾病进展或死亡[事件],或不可接受的毒性),或更长时间(如果发生< 25个事件/队列)。
结果显示, pNET 患者mPFS 5.6 (5.5; 8.3)个月,中肠 NET患者 mPFS 8.3 (5.6; 11.1)个月。事后分析显示,Ki67 ≤10%的 pNET 患者(n=43),mPFS 8.0 (5.6; 8.3)个月。治疗相关AE发生率,pNET组37.5%,中肠NET组51.0%。因AE导致退出研究的pNET组n=2,中肠NET组n=4。该研究提示,在pNET或中肠NET患者中,使用SSA加量治疗是有效的,不会增加AE或降低QoL。在pNET组,Ki67<10%的患者PFS更长。
SSA加量,越来越多地用于NET激素分泌症状控制,以及标准剂量疾病进展后的抗增殖治疗。本研究回顾性收集了使用标准剂量SSA/4周疾病进展的晚期GEP-NET患者,给与SSA加量治疗,即每3周或2周接受长效奥曲肽(LAR)30 mg或兰瑞肽Autogel 120 mg治疗。
16例患者平均年龄65±16岁,均有肝转移,加量的适应症为影像学进展(62.5%)、生物标志物升高(12.5%)或综合征控制不佳(25%)。SSA加量后,有75%的患者达到放射学疾病控制(部分缓解或疾病稳定),中位PFS为36个月。与Si-NETs相比pNETs的PFS显著降低(8m vs 36m,P= 0.041)。Ki-67指数≤5%的NET患者显示PFS明显增高(P= 0.047)。该研究提示, si-NETs或Ki-67指数≤5%的患者,更有可能从SSA加量治疗中获益。
白春梅教授:摘要H14和H17,探讨了SSA加量治疗,作为SSA一线进展后二线治疗的重要价值。CLARINET FORTE兰瑞肽Autogel加量治疗研究,结合先前NETTER-1研究中长效奥曲肽加量治疗组,两项前瞻性研究,以及摘要H17等其他回顾性研究,反复验证了晚期胃肠胰NET SSA一线治疗进展后,选择加量治疗可获得额外PFS,并且不会增加AE或降低QoL。加量治疗可作为SSA一线治疗进展缓慢的患者的治疗选择,可以使患者充分的从SSA这类药物中获益,但不同原发部位以及不同Ki67区间的疗效可能存在差异。
H5: 生长抑素受体显像(SRS)结果并不一定能预测SSA治疗pNET疗效
SRS在预测SSA疗效中的作用仍有很多争议,本研究评估了SRS预测SSA治疗pNET疗效的作用。回顾性分析了复旦大学肿瘤医院胰腺肿瘤科pNET数据库中的122名转移性pNET患者,接受SSA一线单药治疗(长效奥曲肽或兰瑞肽),肝脏肿瘤负荷(HTB)评分1至6分,所有患者进行SRS检测并评估kenning评分。
结果显示, 122例pNET患者,16例(13.1%)为G1级,92例(75.4%)为G2级,14例(11.5%)为G3级。其中105例(86.1%)为SRS阳性,17例(13.9%)SRS阴性。使用SSA治疗的疾病控制率(DCR)与肿瘤负荷(HTB 1&2: 92.9%, HTB 3&4: 57.7%, HTB 5&6: 26.1%,P<0.0001)和分级(G1: 73.3%, G2: 63.7%, G3: 42.8%, G1 vs G3 P=0.048)相关。SSA DCR与SRS显像情况(SRS阳性: 66.7%, SRS阴性: 52.9%, p>0.05)和kenning评分(0-1: 56.2%, 2-4: 66.2%, p>0.05)无显著相关性。中位PFS(m,月)与HTB(HTB 1&2: 75m, HTB 3&4: 47.5m, HTB 5&6: 20.8m, P<0.0001)和分级(G1: NR, G2: 49m, G3: 14m, P=0.048)相关。综上,较低的HTB和分级与SSA治疗预后相关,SRS显像结果并不一定能预测SSA治疗反应。
白春梅教授:SSA通常被推荐用于SSTR阳性的胃肠胰NET患者,而这项来自复旦大学肿瘤医院胰腺肿瘤科的研究,通过对 122名转移性pNET患者的分析,提示SRS显像并不一定能预测SSA治疗反应,而SSA疗效主要与肝脏肿瘤负荷和分级相关。这项研究给了我们启示,那么在排除了肝脏肿瘤负荷和分级的影响下,SRS显像是否可以预测SSA疗效,以及SSTR表达强度是否与SSA疗效相关,这些问题值得进一步研究探讨。
H10:一线治疗后使用SSA维持治疗,用于不可切除的十二指肠-胰腺神经内分泌肿瘤患者
根据欧洲指南,具有侵袭性转移或局部晚期、不可切除、十二指肠-胰腺(DP)NET的患者应接受全身联合化疗,直到病情进展。侵袭性疾病的定义是进展性和/或有症状的转移和/或显著的肝侵犯(30-50%),和/或骨转移。
这项随机、双盲、安慰剂对照的2期研究,评估侵袭性G1-2 DP-NET一线治疗至少2月后接受兰瑞肽Autogel(LAN) 120mg维持治疗的效果。患者以1:1的比例随机分配,每28天接受LAN或安慰剂治疗,直到病情进展或发生毒性反应。主要终点是6个月的PFS%。
53例患者中,81.1%为G2级,90.6%有转移灶,其中29.2%为肝外转移。一线治疗以化疗为主(96.8%)。一线治疗的中位持续时间为4.6 (2.0;7.7) 个月。18.9%的患者PR,81.1%的患者SD。中位随访时间为27.0 (19.5;31.2) 个月。LAN组6个月 PFS%为73.1% (55.3;86.6),安慰剂组为54.2% (35.8;71.8)。中位PFS分别为19.4 (7.6;32.6) 个月和7.6 (3.0;9.0) 个月。安慰剂组的中位总生存期为41.9个月,LAN组未达到。毒性反应为轻度,主要为1-2级。综上,一线治疗侵袭性G1/2 DP-NET后,使用兰瑞肽Autogel 120mg维持治疗有效,但还需要进一步的验证。
白春梅教授:摘要H10, 探讨了一线治疗后使用SSA维持治疗的疗效。对于肿瘤侵袭性高、进展快的pNET患者,常常选用细胞毒性化疗作为一线治疗,而一线治疗后SSA维持治疗是否有效,尚无充分证据。该随机双盲安慰剂对照的研究,证实了一线治疗侵袭性G1/2 DP-NET后,使用SSA维持治疗有效,但还需要进一步的验证。
H12:SSA单药治疗分化良好的G3 NET的有效性
对于SSA治疗高分化G3 NET的疗效研究,既往仅有小样本量的报告。本研究为梅奥诊所18例接受SSA单药治疗转移性/不可切除的高分化G3 NET患者的回顾性分析。入选标准:中心审查病理学证实高分化G3 NET;采用SSA单药治疗;具有可用于评估缓解的放射学数据;从Ga68 -PET-DOTATATE获得SUVmax,以定量SSTR亲合力;通过IHC评估Rb1和p53状态。主要终点是PFS,并根据RECIST 1.1确定最佳总体缓解率。
研究结果显示:尽管中位PFS仅为4.4个月,但55% G3 NET患者在SSA单药治疗期间病情稳定, 有1/3的患者有超过8个月的病情稳定期,3名患者在SSA单药治疗中至少延长了24个月的病情稳定期。
该研究未来分析方向:疾病进展的患者平均SUVmax更高,ki-67指数似乎与PFS、治疗反应性无明显关联;本研究所有肿瘤标本中,P53和RB1均为野生型,与NET高分化基因特征一致;考虑到与细胞毒性化疗相比,SSA具有良好的安全性,可能是一种有吸引力的治疗选择,需要以前瞻性研究进一步探索。
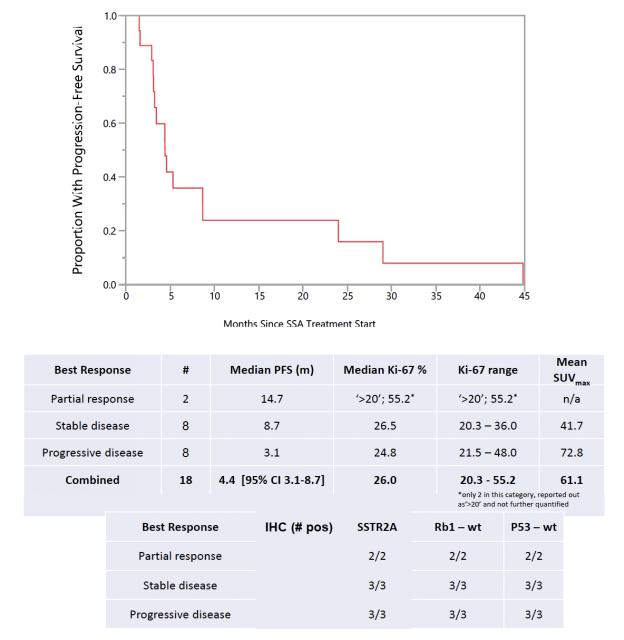
图4 研究结果数据图
Net21021632
白春梅教授:在既往的研究中,SSA治疗晚期G3 NET的抗肿瘤效果有限。但是在该研究中,有部分患者可以获得8个月以上的疾病稳定期,甚至有3个患者获得了超过24个月的疾病稳定期。这提示G3 NET中可能有部分患者可从SSA治疗中获益,但通常不作为一线选择,若不能耐受化疗或靶向治疗,可以考虑SSA治疗。
专家简介
中国医学科学院北京协和医院
肿瘤内科主任
中国临床肿瘤学会理事会理事
中国临床肿瘤学会神经内分泌肿瘤专业委员会主任委员
中国临床肿瘤学会头颈肿瘤专业委员会委员
中国临床肿瘤学会智慧医疗专家委员会常务委员
中国临床肿瘤学会神经内分泌肿瘤专业委员会委员
中国医促会神经内分泌肿瘤分会副主任委员
老年肿瘤学会执行委员
中国研究型医院学会胰腺疾病专业委员会常务委员
擅长领域:抗肿瘤新药的早期研发;肿瘤诊断和治疗,特别是分子标记物在肿瘤诊断、治疗和预后中应用。





 京公网安备 11010502033352号
京公网安备 11010502033352号